Таргетная терапия
Таргетная терапия рака молочной железы
В специальном лечении рака молочной железы используются стандартные методы лечения злокачественных опухолей: хирургия, лучевая терапия и химиотерапия. Все они ведут к гибели опухолевых клеток, но оказывают также неблагоприятное воздействие на здоровые ткани организма, что связано с теми или иными побочными явлениями, иногда достаточно серьезными. Последнее десятилетие отмечено беспрецедентным развитием так называемой ”таргетной терапии” (от “ target”– цель) во всех разделах медицины, основанной на принципе целевого воздействия на фундаментальные молекулярные механизмы, лежащие в основе того или иного заболевания. И более всего этот принцип применим к возникновению и развитию злокачественных опухолей, в основе которых лежат различные нарушения регуляции роста и деления клеток за счет патологии чувствительных центров мембраны клетки (рецепторов), воспринимающих внешние сигналы, нарушения передачи самих этих сигналов, состоящих из множества последовательных биохимических реакций на молекулярном уровне. Таргетная терапия в онкологии основана на изучении и понимании молекулярных механизмов развития той или иной опухоли и разработке препаратов, непосредственно влияющих на специфическую молекулу, которая связана с ростом опухолевых клеток и прогрессированием злокачественного роста. Отсюда второе распространенное название этого вида лечения – “молекулярная таргетная терапия”. Понятно, что такое лечение поражает специфические раковые клетки и в меньшей степени влияет на здоровые ткани, т.е. не обладает выраженными побочными явлениями. Таргетные препараты могут использоваться как самостоятельно, так и в сочетании с традиционными методами лечения опухолей: химиотерапией и радиотерапией.
Лечение рака молочной железы – один из ведущих примеров применения методов с использованием таргетных препаратов, что значительно повысило эффективность как профилактической терапии, так и терапии пациентов с распространенными, метастатическими формами болезни.
Исторически одной из первых “молекулярных целей” таргетной терапии был клеточный рецептор эстрогена – женского полового гормона, который играет важную роль в развитии и течении многих форм рака молочной железы. Присоединение эстрогена к эстроген-рецептору (ЕR) влечет активацию специфических генов, которые стимулируют рост и размножение опухолевой клетки. Исследования показали, что воздействие на клетки, имеющие эстроген-рецепторы (ER – позитивные опухоли), путем блокирования этих рецепторов, является эффективным методом лечения рака молочной железы. Препараты, блокирующие эстроген-рецепторы и препятствующие присоединению эстрогена носят название селективных эстроген-рецептор модуляторов и включают Тамоксифен и Торемифен (Фарестон®). Препарат, Фулвестрант (Фазлодекс®), блокируя эстроген-рецепторы, ведет к их разрушению, что значительно снижает уровень эстроген-рецепторов в клетке.
Другой класс таргетных препаратов, влияющий на рост ER-позитивных опухолей молочной железы представлен “ингибиторами ароматазы”. Ароматаза – специфический белок (энзим) необходимый для выработки эстрогена. Блокирование активности ароматазы ведет к снижению уровня эстрогена в организме, что, в свою очередь, подавляет жизнедеятельность раковых клеток, нуждающихся в эстрогене как стимуляторе роста. Ингибиторы ароматазы применяются у женщин после естественного или индуцированного наступления менопаузы, так как функционирующие яичники способны вырабатывать такое количество ароматазы, что полная ее блокада невозможна. Представителями этого класса препаратов являются Летрозол (Фемара®), Анастрозол (Аримидекс®), Экземестан (Аромазин®).
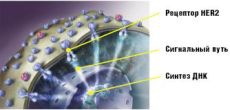
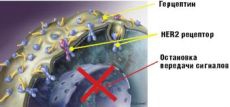
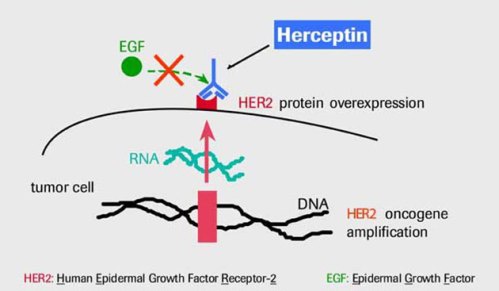
Следующий известный таргетный препарат – Трастузумаб (Герцептин®), “целью” которого служит рецептор человеческого епидермального фактора роста - 2 (human epidermal growth factor receptor 2, сокращенно - Her-2), вырабатывающийся некоторыми видами рака молочной железы и ряда других опухолей. Her-2 является частью механизма передачи сигналoв, ведущих к росту опухолевой клетки (т.н. сигналов - “активаторов роста”). Механизм действия Герцептина до конца не совсем понятен. Высказывается предположение, что, кроме блокады Her-2 на поверхности опухолевых клеток и предотвращения передачи сигналов-активаторов, Герцептин обладает способностью стимулировать иммунную систему организма к атаке клеток, имеющих высокую концентрацию Her-2.
Аналогичной активностью (предотвращение передачи сигналов-активаторов) при лечении опухолей молочной железы, имеющих высокую концентрацию Her-2, обладает препарат Лапатиниб (Тайкерб®), в русской транскрипции – Тайверб®.
В последнее время большой интерес привлекает группа препаратов-ингибиторов (блокаторов) PARP – белка, участвующего в различных клеточных процессах, в основном связанных с восстановлением повреждений ДНК, особенно в опухолевых клетках и так называемой “запрограмированной смертью клетки” или иначе апоптозом. Важность этих лекарств заключается в том, что они действуют в случаях наследственных опухолей с мутацией генов BRCA-1 и BRCA-2 и когда другие основные рецепторы (Her-2, ЕR, PR) опухоль не продуцирует, – так называемых “три-негативных опухолях” молочной железы. Препараты этой группы (Инипариб, Олапариб, Велипариб) сейчас широко исследуются, и уже имеются обещающие результаты их применения. Внедрение этих лекарств в практику будет еще одним успехом таргетнтой терапии опухолей молочной железы.
Иллюстрация:


 LISOD – онкологическая больница с полным циклом помощи: профилактики, диагностики, лечения и реабилитации с использованием международных стандартов на основе доказательной медицины. В LISOD используется необходимое современное высокотехнологичное оборудование для диагностики и лечения онкологических заболеваний.
LISOD – онкологическая больница с полным циклом помощи: профилактики, диагностики, лечения и реабилитации с использованием международных стандартов на основе доказательной медицины. В LISOD используется необходимое современное высокотехнологичное оборудование для диагностики и лечения онкологических заболеваний.
















 LISOD – онкологическая больница с полным циклом помощи: профилактики, диагностики, лечения и реабилитации с использованием международных стандартов на основе доказательной медицины. В LISOD используется необходимое современное высокотехнологичное оборудование для диагностики и лечения онкологических заболеваний.
LISOD – онкологическая больница с полным циклом помощи: профилактики, диагностики, лечения и реабилитации с использованием международных стандартов на основе доказательной медицины. В LISOD используется необходимое современное высокотехнологичное оборудование для диагностики и лечения онкологических заболеваний.
